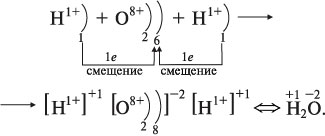
§ 13. Природа и типы химической связи
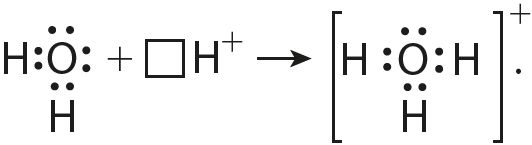
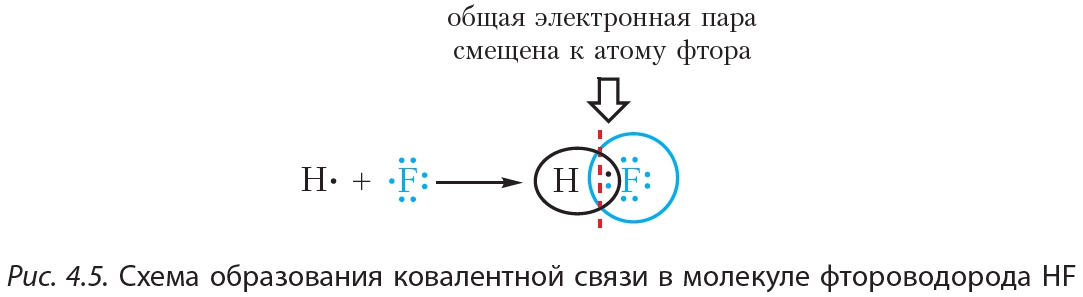
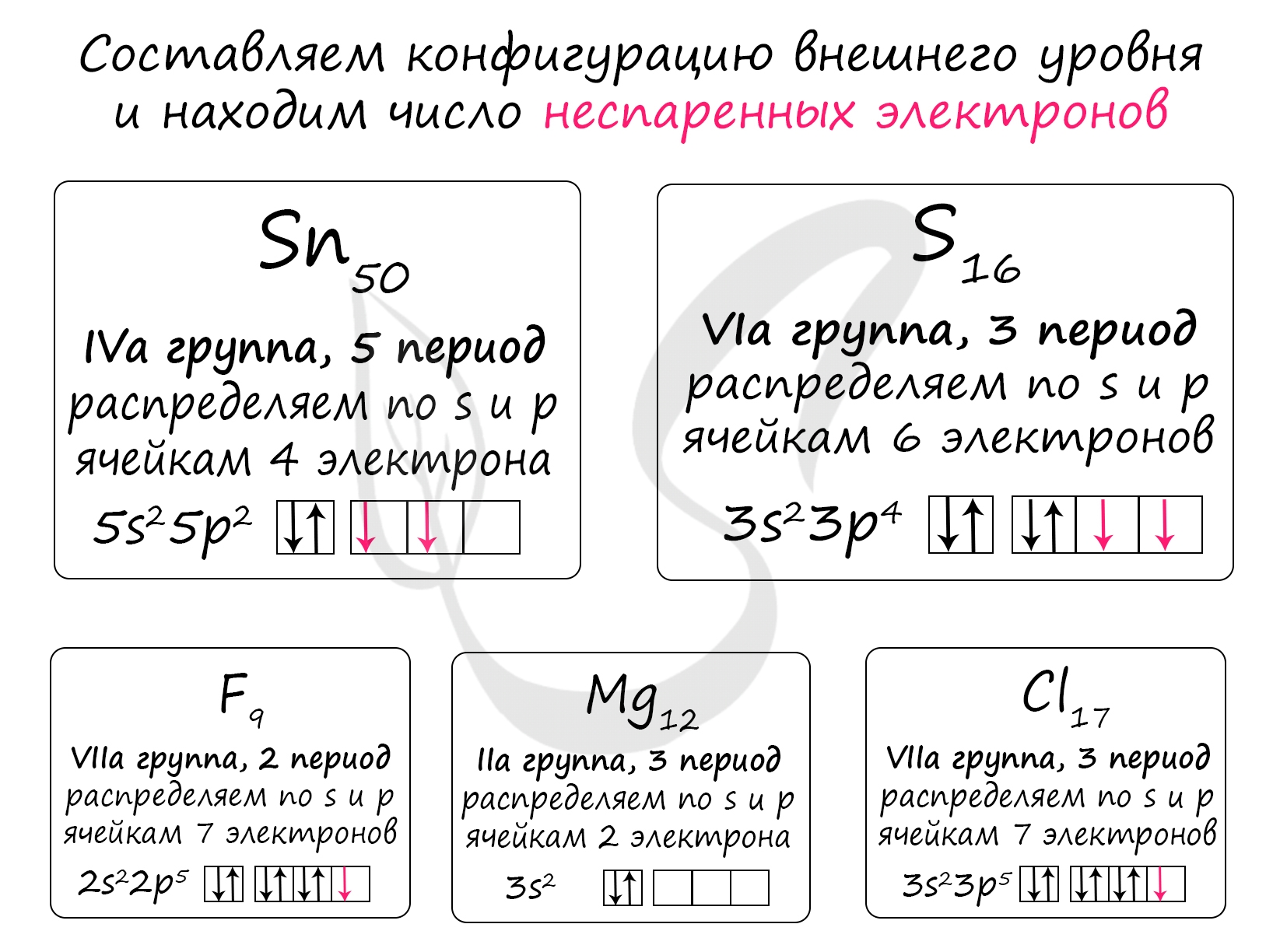
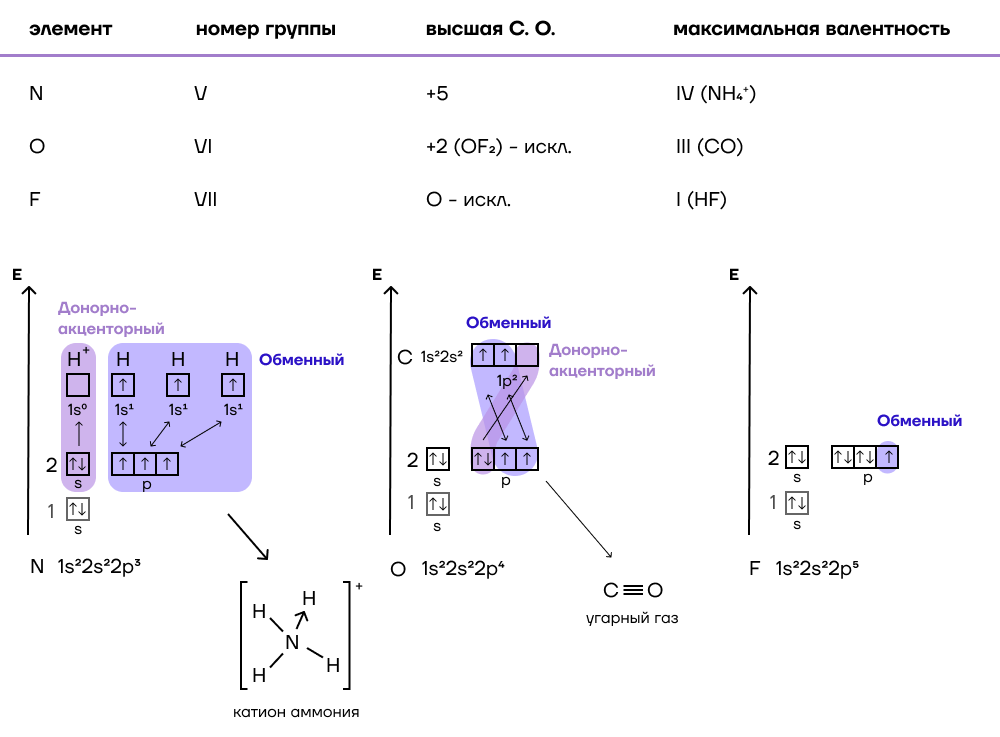
Составьте электронные формулы молекул водорода, хлора, хлороводорода, воды, аммиака и укажите число связывающих и неподелённых электронных пар в каждой из них. Назовите механизм образования связи между атомами, имеющими следующие электронно-графические схемы внешних электронных оболочек:. Согласно приведённой схеме объясните механизм образования ковалентной связи в ионе гидроксония при взаимодействии молекулы воды и иона водорода:.




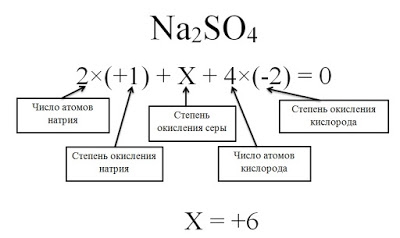
В химии степень окисления элементов говорит о том, как проходят окислительно-восстановительные реакции, а точнее — как при этом атомы перераспределяют между собой электроны. Это не очень сложная тема, но в ней часто бывает путаница. Разберемся, как считать степень окисления в разных соединениях.

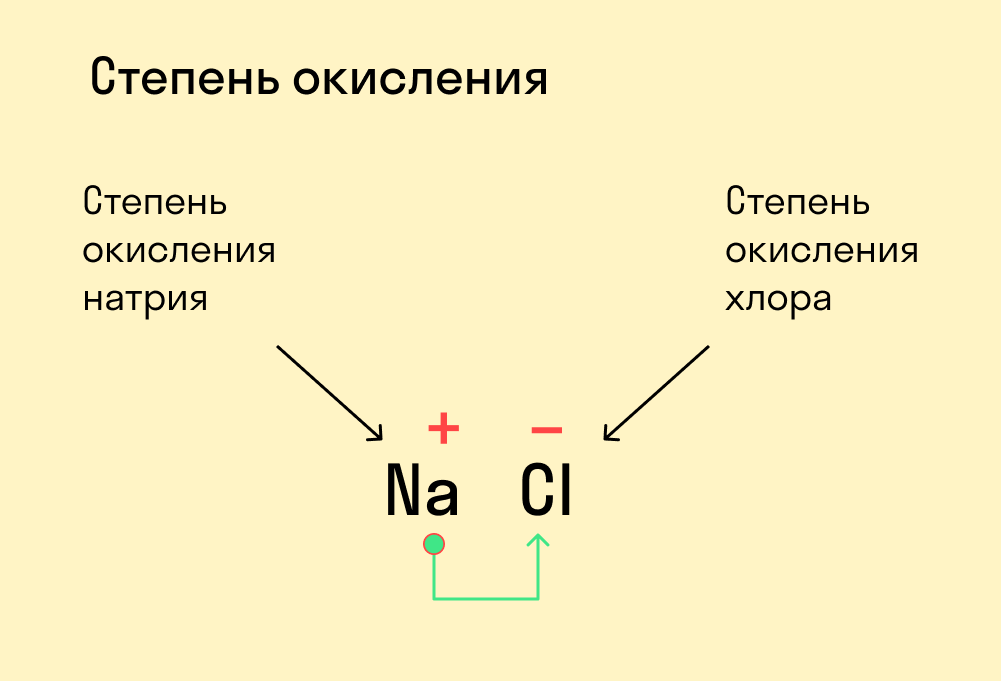
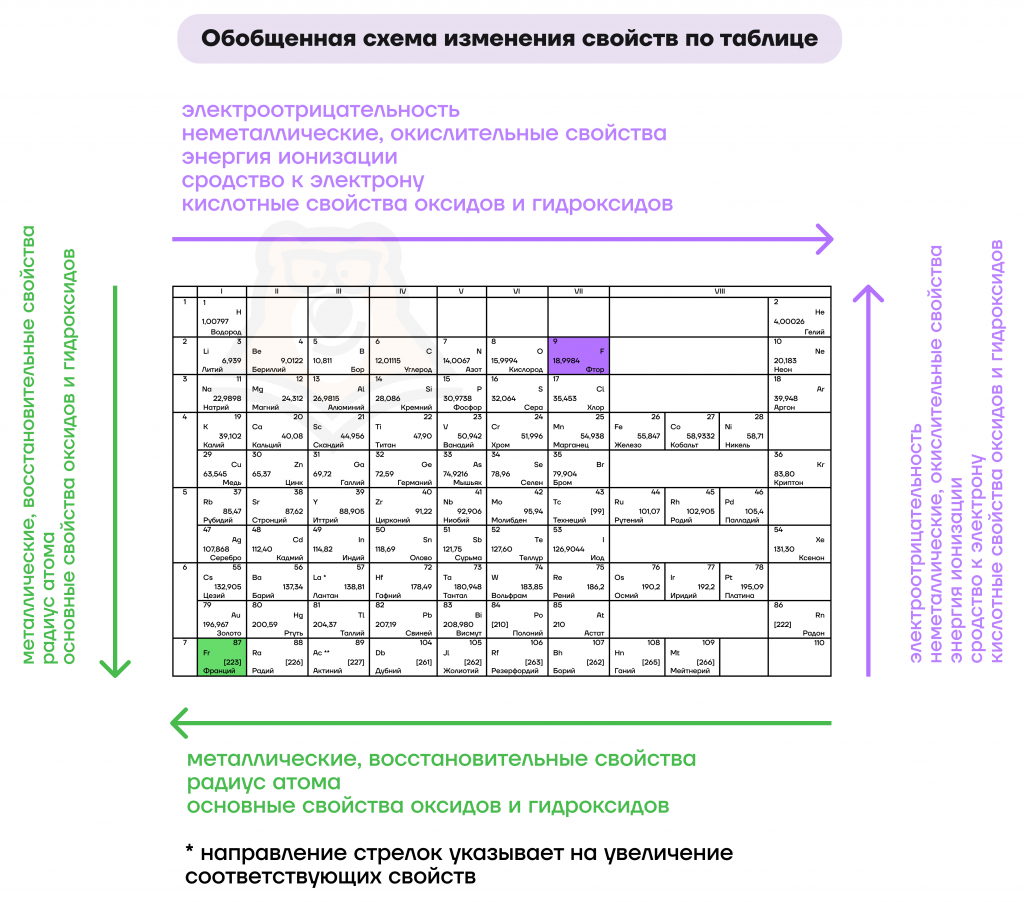
Занимают правый верхний угол Периодической системы элементов Менделеева и обычно отделены линией лесенкой. Количество неметаллов составляет элемента, в зависимости от классификации. Характерной особенностью неметаллов является большее по сравнению с металлами число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов.